Pagina 1 di 1
calore ed entropia
Inviato: 5 set 2011, 20:31
da String
Ciao!
Ho questo dubbio: per calcolare la variazione di entropia per una generica trasformazione irreversibile (supponiamo non adiabatica) dobbiamo riferirci a una trasformazione reversibile che colleghi gli stessi stati iniziale e finale. Ma possiamo effettivamente dire che la quantità di calore scambiata per una tale trasformazione reversibile sia uguale a quella scambiata nella trasformazione irreversibile di partenza?
Re: calore ed entropia
Inviato: 5 set 2011, 20:43
da Pigkappa
String ha scritto:Ma possiamo effettivamente dire che la quantità di calore scambiata per una tale trasformazione reversibile sia uguale a quella scambiata nella trasformazione irreversibile di partenza?
No! Ma questo non inficia il ragionamento.
Il senso è:
1)Non so calcolare la variazione di entropia per una trasformazione irreversibile.
2)Per una trasformazione reversibile, so che è
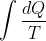
.
3)Lo calcolo con una trasformazione reversibile, e siccome l'entropia è una funzione di stato, il risultato è quello.
Re: calore ed entropia
Inviato: 5 set 2011, 21:10
da String
Faccio un esempio.
Supponiamo che un corpo scambi calore con un altro corpo secondo una generica legge
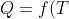)
Per calcolare la variazione di entropia dobbiamo riferirci ad una trasformazione reversibile e calcolare l'integrale
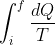
Nel fare questo poniamo
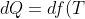)
e risolviamo
}{T})
Ma in generale
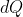
dipende dal tipo di trasformazione e siccome per il calcolo dell'entropia consideriamo una diversa trasformazione, in particolare reversibile fra gli stessi stati iniziale e finale, perchè poniamo il
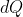
di questa particolare trasformazione uguale al
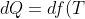)
che abbiamo per la trasformazione irreversibile?
Re: calore ed entropia
Inviato: 6 set 2011, 13:15
da floppino81892
provo a risponderti...anche se stai considerando un processo irreversibile quando trasferisci una quantità elementare di calore
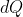
e hai un aumento di temperatura
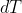
in questo caso il processo è reversibile
ad esempio considera un blocco metallico caldo appoggiato ad uno freddo...è un esempio di trasformazione irreversibile perchè non puoi invertirne il verso..se però metti il blocco su una piastra e aumenti la temperatura della piastra di
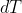
una quantità
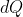
si trasferisce al blocco...se poi diminuisci la temperatura della stessa quantità
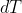
una quantità di calore
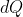
ritorna dal blocco alla piastra e torniamo alle condizioni iniziali...dunque è un processo reversibile
Re: calore ed entropia
Inviato: 6 set 2011, 14:07
da String
floppino81892 ha scritto:anche se stai considerando un processo irreversibile quando trasferisci una quantità elementare di calore
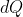
e hai un aumento di temperatura
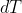
in questo caso il processo è reversibile
ok, ma quindi possiamo affermare che esiste sempre un processo reversibile fra gli stessi stati iniziale e finale che avviene con le stesse modalità di scambio di calore della trasformazione irreversibile che si sta considerando?