in un cilindro termicamente isolato di volume 100 litri contiene una parete mobile sempre a tenuta stagna )che divide il cilindro in 2 parti.
Ciascuna delle due parti contiene un gas perfetto monoatomico alla To=273 K e a pressione 1atm.Una resistenza elettrica scalda il gas nella parte sinistra fino a quando nn ha compresso il gas nella parte destra a 2,5 atm.
Trovare:
1)TEMPERATURA finale nelle due parti
2)Lavoro eseguito dal gas nella parte destra
3)calore fornito dal gas nella parte sinistra
Un cilindro termicamente isolato
-
Donato Palermo
- Messaggi: 13
- Iscritto il: 11 feb 2009, 21:34
Re: Un cilindro termicamente isolato
rispondete questo è a livello regionale
Re: Un cilindro termicamente isolato
Sbaglio o serve sapere come la parete mobile divide il recipiente?
Re: Un cilindro termicamente isolato
Pazzesco... questo problema mi era capitato nel compito di fisica...
Cmq, per quel che ne so io anche la parete dovrebbe essere isolante (altrimenti avremmo bisogno di informazioni riguardo alla sua capacità conduttiva) e quindi la seconda sezione del cilindro viene compressa adiabaticamente.
@Rigel
Sapendo che sono gas perfetti alla stessa temperatura e pressione credo possiamo dedurre che la condizione iniziale sia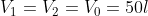
Detto ciò non resta che imporre l'equazione della trasformazione:
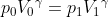
e risolverla; trovato il volume finale della seconda parte del cilindro occorre imporre la condizione che la pressione dev'essere uguale in entrambe le parti a 2,5atm. Poi si ricavano le temperature con l'equazione dei gas perfetti (le moli del gas si ricavano dalle condizioni iniziali) e il lavoro nella seconda sezione del tubo (l'opposto della variazione di energia interna).
Il lavoro nella prima parte è esattamente l'opposto di questo...
Lascio ad uno più esperto in di me l'onere di formule e calcoli...
di me l'onere di formule e calcoli... 
Cmq, per quel che ne so io anche la parete dovrebbe essere isolante (altrimenti avremmo bisogno di informazioni riguardo alla sua capacità conduttiva) e quindi la seconda sezione del cilindro viene compressa adiabaticamente.
@Rigel
Sapendo che sono gas perfetti alla stessa temperatura e pressione credo possiamo dedurre che la condizione iniziale sia
Detto ciò non resta che imporre l'equazione della trasformazione:
e risolverla; trovato il volume finale della seconda parte del cilindro occorre imporre la condizione che la pressione dev'essere uguale in entrambe le parti a 2,5atm. Poi si ricavano le temperature con l'equazione dei gas perfetti (le moli del gas si ricavano dalle condizioni iniziali) e il lavoro nella seconda sezione del tubo (l'opposto della variazione di energia interna).
Il lavoro nella prima parte è esattamente l'opposto di questo...
Lascio ad uno più esperto in
Quando il temperamento originario prevale sulla cultura si è rozzi; quando la cultura prevale sul temperamento originario si è pedanti. Quando la cultura e temperamento si equilibrano, allora si è superiori. (Kong Qiu)
Re: Un cilindro termicamente isolato
no perchè dovremmo sapere il numero di moli in ogni sezione, sebbene anch'io pensi che nel testo originale la parete divida il cilindro in parti uguali..MrTeo ha scritto: Sapendo che sono gas perfetti alla stessa temperatura e pressione credo possiamo dedurre che la condizione iniziale sia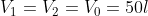
il problema non è chiaro neanche nella terza domanda: che sarebbe il calore fornito dal gas nella parte sinistra?
Re: Un cilindro termicamente isolato
In effetti è vero, da come è stato formulato non abbiamo la certezza dell'uguaglianza dei volumi. Cmq credo che la versione originale non lasciasse dubbi in merito dato che ricordo di non essermi soffermato troppo su queste considerazioni.
Per quanto riguarda il calore credo che non si possa parlare del calore fornito "dal gas" ma "al gas" dalla resistenza... in questo caso basta applicare il primo principio della termodinamica ed è fatto, altrimenti non capisco cosa potrebbe significare.
Per quanto riguarda il calore credo che non si possa parlare del calore fornito "dal gas" ma "al gas" dalla resistenza... in questo caso basta applicare il primo principio della termodinamica ed è fatto, altrimenti non capisco cosa potrebbe significare.
Quando il temperamento originario prevale sulla cultura si è rozzi; quando la cultura prevale sul temperamento originario si è pedanti. Quando la cultura e temperamento si equilibrano, allora si è superiori. (Kong Qiu)
Re: Un cilindro termicamente isolato
Questi sono i risultati che mi trovo. Se qualcun altro l'ha svolto mi farebbe piacere sapere se si trova! 
1) temperatura a sinistra = 971,55 K; temperatura a destra = 393,95 K
2) Lavoro eseguito dal gas nella parte destra = 3363,66 J
3) Calore fornito al gas nella parte sinistra = 22790,57 J
se ho sbagliato qualcosa chiedo scusa in anticipo
1) temperatura a sinistra = 971,55 K; temperatura a destra = 393,95 K
2) Lavoro eseguito dal gas nella parte destra = 3363,66 J
3) Calore fornito al gas nella parte sinistra = 22790,57 J
se ho sbagliato qualcosa chiedo scusa in anticipo
Re: Un cilindro termicamente isolato
i miei risultati sono:
1)
2)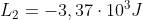
3)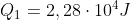
procedimento in breve del primo punto:
-per i due gas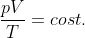 , quindi possiamo ricavare i due volumi finali in funzione delle rispettive temperature finali
, quindi possiamo ricavare i due volumi finali in funzione delle rispettive temperature finali
-la compressione del secondo gas (a destra) è adiabatica, per cui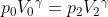 che messo a sistema con l'equazione
che messo a sistema con l'equazione }) precedentemente trovata, ci da la temperatura del secondo gas
precedentemente trovata, ci da la temperatura del secondo gas
-imponendo si ottiene
si ottiene 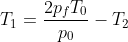
1)
2)
3)
procedimento in breve del primo punto:
-per i due gas
-la compressione del secondo gas (a destra) è adiabatica, per cui
-imponendo
