In questo problema mi sono trovato in disaccordo con la soluzione ufficiale, quindi se qualcuno ha voglia di farlo ( ci vogliono 2 minuti ) magari si può discutere quale soluzione è giusta oppure ( come penso io ) che nessuna soluzione è giusta perchè il problema non ha senso, poi capirete... comunque:
Ci sono due cilindri con pistone mobile identici e posti uno difronte all'altro, il primo (A) contiene 32 kg di argon (massa molare

) mentre il secondo (B) contiene dell ossigeno. I due pistoni sono uniti da una sbarretta rigida e il sistema formato da i due pistoni e la sbarretta ha massa trascurabile. Il cilindro B è in contatto termico con una sorgente ideale a temperatura

mentre il cilindro A è termicamente isolato. Inizialmente i pistoni sono tenuti fermi e l'ossigeno è a pressione
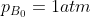
mentre la pressione dell'argon è piu alta. Allora si lascia il pistone e i gas compiono una trasformazione quasi-statica fino all'equilibrio in cui il volume dell'argon è aumentato di otto volte mentre quello dell'ossigeno è diminuito di due volte. Sapendo che la sorgente a contatto con B ha ricevuto una quantità di calore
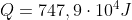
determinare le variabili termodinamiche ( p V T ) dell'argon sia all'inizio che alla fine.
BONUS: un premio speciale a chi capisce a cosa si riferisce il titolo del topic.