Pigkappa ha scritto: ↑18 dic 2023, 4:22
Non ho capito perché è mal posto.
Si tratta di una mera opinione personale. Questo problema non è inedito, dal momento che è contenuto nella sezione "Termodinamica" di molti volumi di Fisica (tra tutti, mi viene in mente
Physics - 9th edition di Cutnell & Johnson, Chapter 15, Problem 33): nella totalità dei casi, la soluzione fornita corrisponde a quella ottenuta considerando adiabatica reversibile la trasformazione in atto (cioè, impiegando la legge
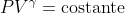
) senza tener conto che non sia possibile soddisfare la condizione per cui la variazione di energia interna del sistema sia nulla, il che è assolutamente errato. A mio giudizio, dunque, gli autori avevano intenzione di formulare il problema implicando che un operatore esterno debba esercitare una forza esterna per controllare manualmente la barriera in movimento, in modo che il processo sia quasi-statico e avvenga in maniera relativamente lenta. Se quest'ultima constatazione non fosse vera, gli stessi estensori avrebbero proposto un problema concettualmente difficile e non completamente risolvibile tramite la Termodinamica classica: bisognerebbe comunque dimostrare che la soluzione più semplice (cioè, quella prevedente l'applicazione della legge dei gas ideali) sia anche l'approssimazione più ragionevole e conduca alla conclusione che la trasformazione è irreversibile. Attuare ciò sarebbe parecchio difficile per un liceale, nonostante non sia impossibile (proverò a dimostrarlo, sempre ammettendo l'infattibilità di giungere alla soluzione esatta).
Pigkappa ha scritto: ↑18 dic 2023, 4:22
Probabilmente l'idea degli autori era di fare un trappolone - molti studenti potrebbero usare
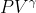
= costante - che però vale solo per le adiabatiche reversibili.
Non si può escludere tale possibilità, pertanto potresti avere ragione. L'argomento del "trappolone", tuttavia, funziona fino ad un certo punto. Nonostante possano essere addotte parecchie prove a sostegno dell'impossibilità di considerare reversibile una trasformazione come quella presentata dal problema in esame, uno studente che abbia affrontato Termodinamica a livelli più o meno alti potrebbe benissimo obiettare che, se la barriera si muovesse a una velocità significativamente inferiore a quella del suono - pari o inferiore ad una bassa percentuale -, la pressione nelle camere avrebbe il tempo di equilibrarsi e il processo sarebbe sufficientemente vicino alla reversibilità da poter essere descritto dall'equazione
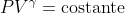
valida per le adiabatiche reversibili: in parecchi libri di Termodinamica viene scritto che "la velocità della barriera dovrebbe essere pari o superiore alla velocità del suono nel gas ideale al momento iniziale, qualora il processo venisse considerato irreversibile", pertanto, continuando nella sua argomentazione, il bravo studente potrebbe asserire che, praticando quest'ultima ipotesi, il volume dovrebbe cambiare a una velocità paragonabile a quella del suono nel gas che, essendo dell'ordine di centinaia di metri al secondo, dovrebbe favorire (assunzione, questa, parecchio improbabile, se non impossibile) un movimento della partizione alla stessa velocità (cioè, centinaia di metri al secondo) perché il processo si discosti in modo significativo da uno approssimativamente reversibile. Tale contro-argomento non è esatto né corretto, ma per confutarlo non sono sufficienti gli strumenti offerti dalla Termodinamica classica e facilmente accessibile: ciò significa che, qualora uno dei candidati avesse esibito un simile ragionamento in occasione dello svolgimento del problema, i membri della commissione giudicatrice avrebbero dovuto introdurre argomenti estremamente avanzati (non alla portata di liceali) per refutare una spiegazione intuitiva apparentemente ragionevole a supporto della tesi della reversibilità del processo.
A questo punto, si profilano due opzioni estremamente contraddittorie e inconciliabili:
1) L'unica possibilità che giustifichi la ragionevolezza e la coerenza del testo del problema risiede nella necessità di non definire la trasformazione termodinamica, escludendo a priori qualsiasi ipotesi di considerazione su reversibilità o irreversibilità di quest'ultima: poiché viene detto soltanto che avviene un "rapido transiente", non è possibile sapere quale tipo di trasformazione abbia luogo durante il processo. Estrapolando l'informazione sul carattere ideale del gas, è sufficiente applicare l'equazione di stato dei gas perfetti e imporre l'uguaglianza delle pressioni nei due compartimenti all'equilibrio finale: il problema, dunque, sarebbe un semplice esercizio prevedente l'applicazione di una legge congiuntamente ad alcune manipolazioni algebriche, senza che possano essere avanzate - eccetto il carattere adiabatico della trasformazione - osservazioni sulla particolare situazione fisica. Rinunciando a conoscere il tipo di processo, si conferisce ad ognuna delle due possibilità (reversibilità e irreversibilità) la medesima percentuale di realizzazione, cosicché la trasformazione possa essere indifferentemente considerata reversibile o irreversibile senza che tale indecisione sortisca effetto sullo svolgimento del problema.
2) D'altro canto, tuttavia, è possibile individuare un (apprezzabile) numero di prove a sostegno della tesi dell'irreversibilità del processo, totalmente corrispondente a quello di argomenti atti a respingere l'idea di reversibilità dello stesso. Questo giudizio è estremamente in disaccordo con il punto precedente. Pertanto, se si accetta la contraddizione, bisogna abbandonare ogni valutazione della situazione fisica e accontentarsi semplicemente di una nota soluzione; se non la si accoglie, è necessario riconoscere il carattere altamente irreversibile del processo e, con esso, la necessità di considerare la (pur corretta) applicazione della legge dei gas perfetti come un'approssimazione (per quanto abbastanza accurata) e l'impossibilità di risolvere il problema
in maniera esatta. In una trasformazione irreversibile, il comportamento di un gas ideale non è descritto dalla legge dei gas ideali (nonostante venga ancora così chiamato), la quale può essere applicata (non necessariamente, però) soltanto all'equilibrio termodinamico, in corrispondenza di stati in cui il gas non si espande o comprime improvvisamente. Anche se gli stati iniziale e finale costituiscono stati di equilibrio termodinamico, ciò non è sufficiente: affinché la legge dei gas ideali sia
perfettamente applicabile, il processo in questione deve essere all'equilibrio termodinamico in tutti gli stati intermedi, ovvero consistere in una sequenza continua di stati di equilibrio termodinamico sull'intero percorso del processo, dimodoché non siano ammessi cambiamenti spontanei che coinvolgano stati di non-equilibrio. Ecco uno dei motivi per cui, in una trasformazione irreversibile, l'impiego di
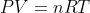
è certamente lecito, ma non fornisce l'
esatta soluzione nemmeno sotto la semplificazione dell'etichetta di "gas ideale": si tratta, come ribadito più volte, di una mera approssimazione di buon grado.
Tale discorso non inficia la correttezza della soluzione di @Higgs (che, tra l'altro, avevo ricavato anche io in forma totalmente analoga), ma mira a constatare la rischiosità insita nella proposta di questo genere di problemi: non reputo infondato affermare che, probabilmente, gli autori del problema ne abbiano sottovalutato la portata, interpretandolo (o ponendolo) male e acconsentendo alla circolazione di un esercizio enormemente più complesso di quanto, in verità, avrebbero voluto che fosse.
Il condensato di constatazioni di cui sopra costituisce soltanto una presentazione delle insidie celate dal problema: qualora tu accettassi e accogliessi la "sfida", potremmo iniziare una discussione più dettagliata sull'interessante situazione fisica.
Pigkappa ha scritto: ↑18 dic 2023, 13:22
Metti che tra la parete mobile, di massa piccola ma non nulla così che il peso poggi sui bordi della scatola, e i bordi interni del contenitore ci sia un coefficiente di attrito
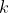
inizialmente infinito, che poi rilassiamo molto lentamente fino a
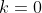
.
Non abbiamo sostanzialmente portato il sistema dallo stato iniziale a quello finale, passando solo da trasformazioni quasistatiche?
Sì, secondo me hai ragione. Le trasformazioni in atto possono essere quasistatiche, purché avvengano abbastanza lentamente da mantenere infinitesimale la differenza di pressione tra le parti, e a patto che non vi siano gradienti di temperatura all'interno di ciascun gas.
= V_B(0)) ma temperature diverse
ma temperature diverse >T_B(0)) . Ad un certo istante, la parete mobile viene lasciata libera di scorrere senza attrito mantenendosi parallela alle basi del cilindro e il sistema, dopo un rapido transiente, raggiunge una nuova posizione di equilibrio.
. Ad un certo istante, la parete mobile viene lasciata libera di scorrere senza attrito mantenendosi parallela alle basi del cilindro e il sistema, dopo un rapido transiente, raggiunge una nuova posizione di equilibrio., P_B(f)) nelle due parti del sistema una volta raggiunta la nuova condizione di equilibrio.
nelle due parti del sistema una volta raggiunta la nuova condizione di equilibrio.