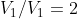Riapro, dopo quasi 13 anni, la trattazione di un argomento (un problema proposto alla prova di ammissione del 2010/11 alla SNS) allo scopo di offrirne una risoluzione che, sebbene facile, può essere utilmente presa in considerazione da chiunque visiti il Forum.
Si consideri, sul piano di Clapeyron
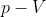
, un ciclo rettangolare
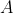
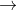
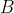
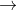
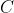
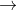
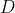
: la trasformazione
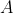
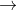
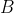
è un'espansione isobara su
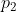
da
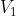
a
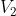
; la trasformazione
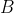
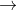
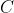
è un'isocora su
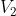
da
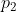
a
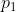
; la trasformazione
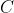
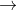
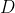
è una compressione isobara su
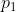
da
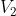
a
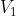
; la trasformazione
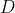
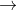
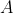
è un'isocora su
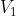
da
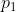
a
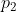
. Pertanto, applicando l'equazione dei gas perfetti ai quattro stati
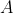
(stato iniziale dell'espansione isobara da
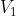
a
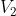
e finale dell'isocora da
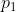
a
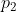
),
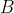
(stato finale dell'espansione isobara da
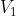
a
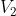
e iniziale dell'isocora da
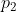
a
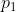
),
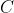
(stato finale dell''isocora da
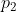
a
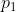
e iniziale della compressione isobara da
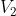
a
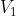
),
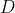
(stato finale della compressione isobara da

a
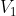
e iniziale dell'isocora su
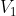
da
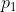
a
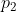
):
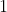)
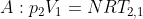
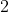)
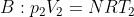
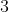)
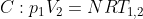
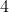)
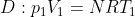
Dalla
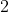)
, è possibile ottenere
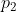
:
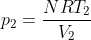
Dalla
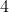)
, è possibile ottenere
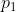
:
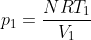
Inoltre, si possono ricavare le temperature intermedie
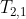
e

, dividendo rispettivamente la
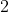)
dalla
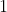)
, e la
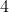)
dalla
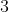)
. Dunque:


)
Per definizione, il rendimento
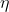
del ciclo termodinamico rettangolare
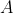
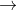
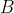
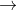
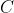
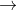
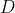
, che avviene tra la temperatura minima
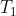
(dello stato D) e quella massima

(dello stato B), si calcola come:
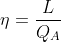
, dove
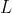
è il lavoro compiuto e

è il calore assorbito durante il ciclo.
Poiché il ciclo
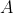
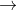
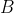
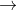
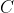
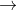
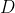
è rettangolare e percorso in senso orario, il lavoro
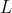
è - per convenzione - positivo; esso può essere calcolato come area del rettangolo
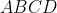
deducibile dal diagramma
)
, le cui base e altezza sono pari, rispettivamente, a
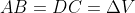
e
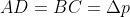
, ove

e
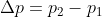
. Si ottiene, dunque:
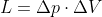
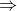
 (V_2 - V_1))
Sostituendo
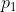
e
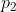
nell'espressione di
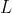
, è possibile esprimere il lavoro in funzione delle temperature
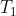
e
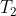
:
 \bigg(V_2 - V_1\bigg))

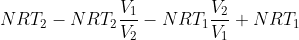

 - NRT_1 \bigg(\frac{V_2}{V_1} - 1\bigg))
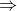
T_2 -\bigg(\frac{V_2}{V_1}-1\bigg)T_1\bigg])
, espressione nella quale si è introdotto il rapporto tra i volumi anziché quello tra le pressioni.
Il calore

assorbito durante le trasformazioni
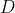
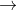
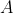
(isocora, cioè a volume costante) e
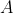
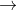
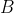
(isobara, cioè a pressione costante), è dato da:
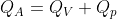
, dove
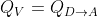
è il calore assorbito durante l'isocora e

il calore assorbito durante l'isobara. I calori
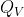
e
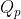
possono essere calcolati come:
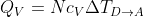
e
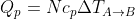
, dove
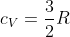
e
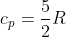
rappresentano, rispettivamente, i calori molari a volume e pressione costanti per un gas monoatomico, con:
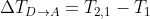
e
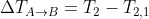
. Dunque:
 + \frac{5}{2} NR \bigg(T_2 - T_{2,1}\bigg))
.
Sostituendo i valori delle temperature intermedie
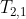
e

trovate in precedenza, si ottiene:
 + \frac{5}{2} NR \bigg(T_2-\frac{V_1}{V_2}T_2\bigg))

)

)
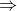
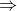
 T_2 -\frac{3}{2} T_1\bigg])
Il rendimento del ciclo sarà, dunque:
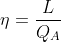

T_2 -\bigg(\frac{V_2}{V_1}-1\bigg)T_1\bigg]}{NR \bigg[\bigg(\frac{5}{2}-\frac{V_1}{V_2}\bigg) T_2 -\frac{3}{2} T_1\bigg]})
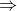
T_2 -\bigg(\frac{V_2}{V_1}-1\bigg)T_1\bigg]}{ \bigg[\bigg(\frac{5}{2}-\frac{V_1}{V_2}\bigg) T_2 -\frac{3}{2} T_1\bigg]})
Dividendo, per ragioni dimostrative, numeratore e denominatore per il coefficiente di
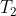
al numeratore, ovvero
)
, il rendimento presenterà un'espressione analitica uguale alla seguente:
T_2 -\bigg(\frac{V_2}{V_1}-1\bigg)T_1\bigg]}{\bigg(1-\frac{V_1}{V_2}\bigg)}}{\frac{\bigg[\bigg(\frac{5}{2}-\frac{V_1}{V_2}\bigg) T_2 -\frac{3}{2} T_1\bigg]}{\bigg(1-\frac{V_1}{V_2}\bigg)}})

T_1}{\bigg(1-\frac{V_1}{V_2}\bigg)}}}{\frac{\bigg(\frac{5V_2 -2V_1}{2V_2}\bigg)T_2}{\frac{V_2-V_1}{V_2}}-\frac{3T_1}{2\bigg(\frac{V_2-V_1}{V_2}\bigg)}} = \frac{T_2-\bigg(\frac{\frac{V_2-V_1}{V_1}}{\frac{V_2-V_1}{V_2}}\bigg)T_1}{\bigg[\frac{5V_2-2V_1}{2 (V_2 - V_1)}\bigg]T_2 - \bigg [\frac{3V_2}{2(V_2 -V_1)}\bigg]T_1})
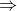
}\bigg]T_2 - \bigg [\frac{3V_2}{2(V_2 -V_1)}\bigg]T_1}})
Dal confronto tra il rendimento termodinamico del ciclo reversibile rettangolare in esame e quello di un ciclo di Carnot operante tra le stesse temperature estreme
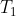
e
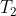
, ci si aspetta che il primo sia strettamente inferiore al secondo, dal momento che il rendimento del ciclo di Carnot è superiore a quello di qualsiasi macchina termica reale.
In tali condizioni termiche, un ciclo di Carnot ha rendimento:
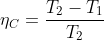
,
perciò, prevedendo che
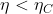
(cioè, che il rendimento del ciclo di Carnot è sempre strettamente maggiore di quello del ciclo
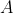
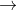
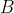
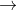
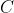
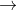
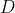
), dovrà auspicabilmente valere che: I) il numeratore di
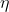
,
)
sia strettamente minore di quello di

,
)
; II) che il denominatore di
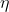
,
}\bigg]T_2 - \bigg [\frac{3V_2}{2(V_2 -V_1)}\bigg]T_1} \bigg\})
, sia strettamente maggiore di quello di

,
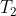
: riguardo quest'ultima condizione, in caso contrario, si otterrebbe il cambiamento di verso della disuguaglianza che si vuole ottenere (e ciò destituirebbe la ragionevole ipotesi iniziale di ogni fondamento).
Si giunga alle asserzioni I) e II) attraverso una serie di osservazioni a monte, che prevedono catene di disuguaglianze:
I)
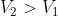
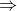
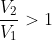
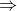

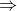
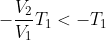
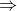
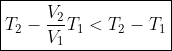
. Dunque, il numeratore di
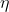
è minore di
)
, numeratore di

, in quanto si toglie a
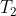
una quantità maggiore di
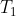
.
II)
}\bigg]T_2 - \bigg [\frac{3V_2}{2(V_2 -V_1)}\bigg]T_1 - T_2)

}-1 \bigg] T_2 - \bigg [\frac{3V_2}{2(V_2 -V_1)}\bigg]T_1)

} \bigg] T_2 - \bigg [\frac{3V_2}{2(V_2 -V_1)}\bigg]T_1)

} \bigg] T_2 - \bigg [\frac{3V_2}{2(V_2 -V_1)}\bigg]T_1)

} \bigg] \bigg(T_2-T_1 \bigg) > 0)
, poiché
} \bigg] > 0)
in quanto rapporto di valori sempre positivi e
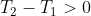
in quanto
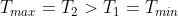
.
Per cui, essendo
}\bigg]T_2 - \bigg [\frac{3V_2}{2(V_2 -V_1)}\bigg]T_1 - T_2)

} \bigg] \bigg(T_2-T_1 \bigg))
, allora:
}\bigg]T_2 - \bigg [\frac{3V_2}{2(V_2 -V_1)}\bigg]T_1 - T_2 > 0)
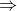
}\bigg]T_2 - \bigg [\frac{3V_2}{2(V_2 -V_1)}\bigg]T_1 > T_2})
.
Quindi, in virtù delle considerazioni precedenti, si ha - come ci si aspettava - che:

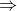

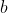)
Si dimostri esplicitamente la relazione precedente (per la quale il rendimento

del ciclo di Carnot operante tra
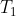
e

è maggiore di quello
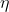
del ciclo reversibile) nel caso particolare

. Avendo espresso
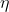
in funzione del quoziente dei volumi, agevole risulta l'esplicita attestazione dell'asserto del punto
)
nel caso particolare poc'anzi riportato. Infatti, ponendo

, ovvero

, nell'espressione di
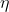
, si ottiene:
}\bigg]T_2 - \bigg [\frac{3V_2}{2(V_2 -V_1)}\bigg]T_1})

)

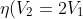 = \frac{T_2 -\frac{2V_1}{V_1}T_1}{\bigg[\frac{10V_1 - 2V_1}{2 (2V_1 - V_1)}\bigg]T_2 - \bigg [\frac{6V_1}{2(2V_1 -V_1)}\bigg]T_1})

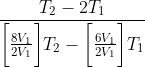
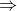
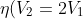 = \frac{T_2 -2 T_1}{ 4T_2 - 3 T_1})
.
Ancora una volta, si può dimostrare che il numeratore di
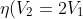)
, ovvero
)
, è minore di quello di

, cioè
)
; e, parimenti, che il denominatore di
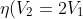)
, ovvero
)
, è maggiore di quello di

, cioè
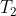
.
I)

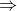
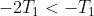
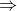
 < (T_2 - T_1)})
II)
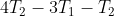

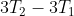

 > 0)
, dunque:

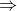
 > T_2})
.
Dunque, si può concludere che:
 < \eta_C})
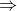
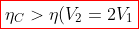})
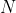 moli compie un ciclo termodinamico, composto da: un espansione isobara alla pressione
moli compie un ciclo termodinamico, composto da: un espansione isobara alla pressione 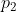 da
da 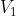 a
a 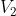 , un'isocora su
, un'isocora su 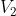 da
da 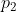 a
a 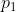 , una compressione isobara su
, una compressione isobara su 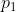 da
da 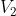 a
a 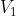 . (In pratica ti davano il piano cartesiano col rettangolino che rappresentava la trasformazione). Si chiede a) di calcolare il rendimento del ciclo e di confrontarlo con quello di una macchina di Carnot che lavora tra le stesse temperature, e b) di verificare direttamente che il rendimento di un ciclo di carnot è sempre maggiore di questo per
. (In pratica ti davano il piano cartesiano col rettangolino che rappresentava la trasformazione). Si chiede a) di calcolare il rendimento del ciclo e di confrontarlo con quello di una macchina di Carnot che lavora tra le stesse temperature, e b) di verificare direttamente che il rendimento di un ciclo di carnot è sempre maggiore di questo per