Il sistema in considerazione è la stanza. Suppongo inoltre che, dato che è un test di ammissione alla Normale, si consideri l'aria un gas perfetto. A meno che le pareti non siano di gomma

, dall'equazione di stato si trova che la quantità

(T in Kelvin) è una costante del processo termodinamico.
L'aria può essere supposta un gas perfetto biatomico, infatti è formata prevalentemente (>90%) da molecole di
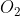
e
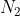
. L'energia interna per mole dell'aria, in funzione della temperatura, si può quindi supporre

(T in Kelvin).
A questo punto,

, analogamente

e
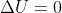
.
Se si fornisce al gas una quantità di calore (infinitesima)
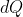
, esso aumenta la propria temperatura di
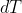
, e il processo è isobaro, quindi

. Si ha quindi

.
Dalla relazione di Meyer,

, si ha

quindi

.