Una mole di azoto
)
occupa inizialmente un volume
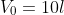
alla temperatura
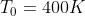
. Il gas compie una trasformazione adiabatica irreversibile a seguito della quale il volume raddoppia. Il lavoro compiuto dal gas durante la trasformazione è
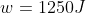
.
Determinare la temperatura
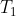
e la pressione
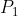
del gas una volta raggiunto l'equilibrio termodinamico.
Per il calcolo di
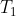
, seguendo due strade diverse trovo due risultati diversi... non riesco a capire dove stia l'inghippo.
Il metodo più veloce che viene in mente, è quello di usare la classica formula per la trasformazione adiabatica da cui si può ricavare:
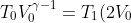^{\gamma-1})
Ottenendo così
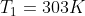
Usando invece il primo principio della termodinamica:
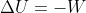
=-W)
Da cui si ottiene

Perchè? Dove sta l'errore? Bisogna trarre qualche informazione dal fatto che è irreversibile?



