Helio98 ha scritto:Considerando il classico sistema del pistone, il lavoro del sistema per un'espansione si calcola integrando W=pdv
Giusto.
Helio98 ha scritto:Nel caso di un'espansione irreversibile si usa la pressione esterna. Essendo il lavoro una forma di scambio energetico il lavoro che fa il sistema è uguale al lavoro che l'ambiente subisce e capisco l'uso della pressione esterna perché quella interna non è definibile in ogni istante.
Questo sinceramente non mi convince. Di solito in termodinamica si assume che la pressione interna e quella esterna siano (quasi) uguali. In questo modo la forza sul pistone e' (quasi) nulla e il pistone si muove lentamente su e giu'.
Se la pressione esterna e interna non sono (quasi) uguali, il pistone accelera e il moto del pistone e del gas sono complicati. In questo caso usciamo dall'ambito della termodinamica e entriamo nell'ambito della fluidodinamica che e' ben piu' complessa.
Ci sono trasformazioni irreversibili in cui si puo' comunque dire che la pressione interna ed esterna sono quasi uguali. Un caso potrebbe essere quello di una trasformazione chimica nel gas che fa si' che energia potenziale chimica si trasformi in calore. La maggior parte dei problemi sulle trasformazioni irreversibili che vengono posti in termodinamica dovrebbe essere di questo tipo.
Helio98 ha scritto:Quello che mi chiedo, ma non ne trovo la conferma, è se nell'espansione è come se non tutta la pressione interna del gas contribuisca a fare lavoro, altrimenti matematicamente non mi trovo che il lavoro del sistema è uguale a quello subito dall'ambiente.
Per l'appunto, il lavoro fatto dal gas deve essere uguale e opposto a quello fatto dal sistema esterno, altrimenti il pistone ha una velocita' non nulla alla fine del processo. E il lavoro fatto dal gas e' indubbiamente
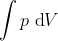
dove
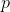
e' la pressione del gas che sta a contatto con il pistone (sottolineo:
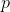
e' la pressione interna, non solo una sua parte). A meno di situazioni piu' complicate di quelle che vuoi trattare tu,
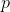
e' la stessa in ogni punto del gas.
Non so se ti stai riferendo a una situazione particolare oppure hai trovato un libro che dice qualcosa di confuso su questi argomenti; non riesco a immaginare casi in cui la pressione interna
non è definibile in ogni istante ma in cui possiamo comunque usare semplici regole di termodinamica invece che di fluidodinamica.
"Per un laser, si passa da temperature positive a temperature negative non passando attraverso 0 K, ma passando attraverso l'infinito!" (cit.)
"Perché dovremmo pagare uno scienziato quando facciamo le migliori scarpe del mondo?" (cit.)
