Posto il mio procedimento...
Analisi teorica: Questo è un caso che si può paragonare al tipico esempio che si fa per calcolare la probabilità dell'entropia, cioè quello di una scatola divisa in due parti uguali. Come una particella dentro la scatola può andare a destra o a sinistra, allo stesso modo in questo problema una particella può avere due diversi tipi di energia..Ora ci chiediamo, quale è la probabilità di trovare la particella in una delle due energie?? Che equivale a, quante particelle troveremmo mediamente ad un livello di energia e quante nell'altro se avessimo a disposizione tantissime particelle ed esse raggiungessero l'equilibrio??
Nel tipico esempio della scatola la risposta sarebbe, metà del tutto da una parte e metà dall'altra! Questo è lo stato più probabile che di conseguenza secondo la
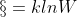
, porta all'entropia maggiore. Il problema che ci si pone qui invece è più arduo, perchè le energie non sono "equispaziate" come nella scatola, cioè potrebbe essere che invece di 1/2 e 1/2 potremmo trovare 1/3 e 2/3 ecc.. e tutto dipende dalla temperatura in questione. Faccio un esempio. Se la temperatura di equilibrio fosse associata all energia
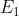
allora vi sarebbe equilibrio e quindi l'entropia sarebbe massima solo nel caso in cui tutte le particelle andassero a quella temperatura e quindi a quella energia.
Procedimento:
Allora all'inizio
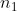
particelle avranno un'energia pari a
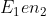
particelle avranno un'energia pari a
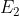
, quindi l'energia totale dell'universo sarà
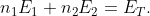
Quando però colleghiamo all'universo un serbatoio di energia, che considereremo come ambiente, tra le particelle e il serbatoio si susseguono scambi di energia fino a quando il sistema delle n particelle non avrà raggiunto l'equilibrio termico. L'energia del sistema quindi non si conserva bensì varia..aumentando o diminuendo. Tutto dipende dalla temperatura
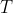
di equilibrio. Kmq quello che interessa per la soluzione del problema è sapere che l'energia varia di

che in questo caso è sempre di
)
. Quindi in totale ci saranno
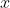
variazioni positivi(assorbimento) o
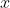
variazioni negativi(cessioni) di energia dal sistema all'ambiente.
Ora sfruttando la definizione statistica di entropia avremo che:
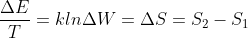
dove
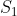
lo possiamo prendere anche considerando un caso estremo in cui tutte le particelle "stanno da una parte" cioè hanno la stessa energia ad esempio
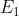
.. quindi
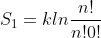
Allora i conti si semplificano ed
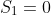
Non resta che calcolare
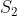
n_2 \over T}=kln \frac {n!}{n_1!n_2!})
e da qui iniziano una marea di calcoli da cui per ora non riesco a venirne fuori....


Ippo ha scritto:Gauss91 ha scritto:Nella mia suprema ignoranza, secondo me l'equilibrio si ha quando l'entropia assume il massimo valore possibile. Per il secondo principio della termodinamica...
Ok. E quindi: quando una particella salta da uno stato all'altro, che cosa ci aspettiamo che faccia l'entropia globale?
Se ne deduce che aumenta.
La fisica è come il sesso: certamente può fornire alcuni risultati pratici, ma non è questo il motivo per cui lo facciamo!
-Richard Feynman