ma provate ad analizzare un processo singolo!!Loren Kocillari89 ha scritto: Ok, se il macrostato iniziale stà tutto da una parte e l'entropia iniziale è 0, il macrostato finale sarà:, dove t è il numero di "pacchetti d'energia" scambiati.:
Equilibrio termico di particelle a due stati
Re: Equilibrio termico di particelle a due stati
- Loren Kocillari89
- Messaggi: 173
- Iscritto il: 16 gen 2009, 18:37
Re: Equilibrio termico di particelle a due stati
partendo dalla scritta di sopra si avrà:
/T=k ( \ln P_1- \ln P_2)) , con
, con 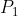 e
e 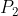 rispettivamente le probabilità di avere n_1 particelle all'energia E_1 ed n_2 all'energia E_2.
rispettivamente le probabilità di avere n_1 particelle all'energia E_1 ed n_2 all'energia E_2.
ora sfrutto la cosiddetta densità di probabilità e ho: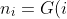P_i)
sostituendo tutto si ha:)=e^{(E_i/ Tk)})
infine
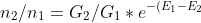/kT})
Dimmi che non era questa la soluzione...
ora sfrutto la cosiddetta densità di probabilità e ho:
sostituendo tutto si ha:
infine
Dimmi che non era questa la soluzione...
Ultima modifica di Loren Kocillari89 il 6 ago 2010, 20:22, modificato 1 volta in totale.
La fisica è come il sesso: certamente può fornire alcuni risultati pratici, ma non è questo il motivo per cui lo facciamo!
-Richard Feynman
-Richard Feynman
Re: Equilibrio termico di particelle a due stati
Hem ok, dopo l'incomprensione iniziale, ho fatto un ragionamento simile a quello che (mi sembra di aver capito) avete fatto anche voi. Anche se il problema è praticamente finito, e visto che con le pagine precedenti si rischia di confondersi le idee, lo scrivo, in modo da fare una sorta di riassunto.
Quando il sistema è all'equilibrio, ogni trasformazione non deve portare ad una variazione di entropia nel sistema, visto che all'equilibrio non ci sono scambi netti di calore. Per un singolo salto energetico da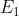 a
a 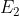 si ha che la variazione di entropia statica delle particelle è
si ha che la variazione di entropia statica delle particelle è = k \ln \left( {W_f \over W_i}\right)) . L'energia fornita dalla sorgente è
. L'energia fornita dalla sorgente è ) , percui la variazione di entropia nella sorgente è
, percui la variazione di entropia nella sorgente è  \over T}) . Come si è detto prima si deve avere
. Come si è detto prima si deve avere 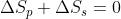 , perciò
, perciò = {(E_2 - E_1) \over T} \rightarrow {W_f \over W_i}= e^{{(E_2 - E_1) \over k T}}) .
.
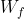 e
e 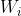 rappresentano tutti i possibili modi di poter prendere rispettivamente
rappresentano tutti i possibili modi di poter prendere rispettivamente ) e
e 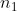 particelle sulle
particelle sulle 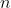 totali. Perciò
totali. Perciò
!(n_2 + 1)!}={n! \over n_1! n_2!}{n_1 \over (n_2 +1)} \approx {n! \over n_1! n_2!}{n_1 \over n_2 })

Infine si ha quindi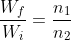 percui
percui 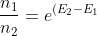 \over k T}})
Quando il sistema è all'equilibrio, ogni trasformazione non deve portare ad una variazione di entropia nel sistema, visto che all'equilibrio non ci sono scambi netti di calore. Per un singolo salto energetico da
Infine si ha quindi
- Loren Kocillari89
- Messaggi: 173
- Iscritto il: 16 gen 2009, 18:37
Re: Equilibrio termico di particelle a due stati
unico appunto. non penso sia lecito approssimare 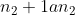 ..non sai a priori quanto vale n_2 allo stato di equilibrio. Kmq mi sembra che ormai il problema è risolto.
..non sai a priori quanto vale n_2 allo stato di equilibrio. Kmq mi sembra che ormai il problema è risolto.
La fisica è come il sesso: certamente può fornire alcuni risultati pratici, ma non è questo il motivo per cui lo facciamo!
-Richard Feynman
-Richard Feynman
Re: Equilibrio termico di particelle a due stati
l'approssimazione è lecita perché stiamo sempre parlando di un "gas" (tante particelle), ma anche se non lo fosse non cambierebbe molto; ci interessava più che altro il tipo di dipendenza dalla temperatura e dalla differenza di energia.
Il risultato che abbiamo ottenuto in questo modo è molto generale. Capita spesso ad esempio in chimica di incontrare formule del tipo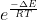 con
con  un qualche salto energetico tra due stati o due fasi o altro; la ragione è collegata a questo tipo di fenomeni (chiaramente per approfondire la cosa serve la meccanica statistica, ma nel frattempo abbiamo ottenuto un bel risultato "a mano").
un qualche salto energetico tra due stati o due fasi o altro; la ragione è collegata a questo tipo di fenomeni (chiaramente per approfondire la cosa serve la meccanica statistica, ma nel frattempo abbiamo ottenuto un bel risultato "a mano").
Note sul risultato: diciamo che sia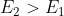 ; allora per
; allora per 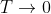 tutte le particelle stanno nello stato 1, quello meno energetico. Questo è ragionevole. Invece per
tutte le particelle stanno nello stato 1, quello meno energetico. Questo è ragionevole. Invece per 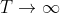 l'esponente va a 0 e l'esponenziale quindi a 1; abbiamo al limite
l'esponente va a 0 e l'esponenziale quindi a 1; abbiamo al limite 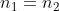 . Anche questo è ragionevole perché per alte T la differenza tra i due livelli diventa trascurabile e ci ritroviamo banalmente con la "scatola divisa a metà" a cui qualcuno ha accennato all'inizio: è equiprobabile stare di qua o di là. NON accade invece MAI, nemmeno per alte T, che tutte le particelle tendano a stare nel livello più energetico, come uno potrebbe pensare ingenuamente "per simmetria" rispetto al limite di T piccole.
. Anche questo è ragionevole perché per alte T la differenza tra i due livelli diventa trascurabile e ci ritroviamo banalmente con la "scatola divisa a metà" a cui qualcuno ha accennato all'inizio: è equiprobabile stare di qua o di là. NON accade invece MAI, nemmeno per alte T, che tutte le particelle tendano a stare nel livello più energetico, come uno potrebbe pensare ingenuamente "per simmetria" rispetto al limite di T piccole.
Il risultato che abbiamo ottenuto in questo modo è molto generale. Capita spesso ad esempio in chimica di incontrare formule del tipo
Note sul risultato: diciamo che sia
- Loren Kocillari89
- Messaggi: 173
- Iscritto il: 16 gen 2009, 18:37
Re: Equilibrio termico di particelle a due stati
Provate ad immaginare cosa accadrebbe se si venisse a scoprire che in una regione dell'universo le particelle tendono a stare nella loro massima energia...Ippo ha scritto: NON accade invece MAI, nemmeno per alte T, che tutte le particelle tendano a stare nel livello più energetico, come uno potrebbe pensare ingenuamente "per simmetria" rispetto al limite di T piccole.
La fisica è come il sesso: certamente può fornire alcuni risultati pratici, ma non è questo il motivo per cui lo facciamo!
-Richard Feynman
-Richard Feynman
Re: Equilibrio termico di particelle a due stati
Nota: avevo provato a quotare il messaggio di Loren sopra ma ho fatto confusione con le opzioni di moderazione e purtroppo l'ho modificato per sbaglio. Ho provato a rimetterlo a posto ma non sono riuscito a fare meglio di così.
Comunque, volevo quotarlo per chiedere:
Comunque, volevo quotarlo per chiedere:
Cosa sono i G(i)?loren ha scritto:ora sfrutto la cosiddetta densità di probabilità e ho:
"Per un laser, si passa da temperature positive a temperature negative non passando attraverso 0 K, ma passando attraverso l'infinito!" (cit.)
"Perché dovremmo pagare uno scienziato quando facciamo le migliori scarpe del mondo?" (cit.)
"Perché dovremmo pagare uno scienziato quando facciamo le migliori scarpe del mondo?" (cit.)
- Loren Kocillari89
- Messaggi: 173
- Iscritto il: 16 gen 2009, 18:37
Re: Equilibrio termico di particelle a due stati
Tranquillo ho rimesso come era primaPigkappa ha scritto:Nota: avevo provato a quotare il messaggio di Loren sopra ma ho fatto confusione con le opzioni di moderazione e purtroppo l'ho modificato per sbaglio. Ho provato a rimetterlo a posto ma non sono riuscito a fare meglio di così.
kmq quella G(i) proviene da questo qui: http://www.unisi.it/fisica/dip/dida/fta ... sMod11.pdf
Sinceramente non ho una teoria sotto per poter dire che funziona come deve, ma se il testo lo ha posto e non mi era sembrato un paraddosso allora l'ho messo...XD
La fisica è come il sesso: certamente può fornire alcuni risultati pratici, ma non è questo il motivo per cui lo facciamo!
-Richard Feynman
-Richard Feynman
Re: Equilibrio termico di particelle a due stati
L'ho chiesto perchè ho già trovato quelle 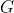 da qualche parte ma non ho mai scoperto cosa fossero. A quanto pare leggendo in quelle dispense si tratta di un coefficiente numerico che si spiega con la fisica quantistica (ergo è lecito che io non lo sappia ancora) e che non è certamente nel programma olimpico (nè ci va vicino).
da qualche parte ma non ho mai scoperto cosa fossero. A quanto pare leggendo in quelle dispense si tratta di un coefficiente numerico che si spiega con la fisica quantistica (ergo è lecito che io non lo sappia ancora) e che non è certamente nel programma olimpico (nè ci va vicino).
"Per un laser, si passa da temperature positive a temperature negative non passando attraverso 0 K, ma passando attraverso l'infinito!" (cit.)
"Perché dovremmo pagare uno scienziato quando facciamo le migliori scarpe del mondo?" (cit.)
"Perché dovremmo pagare uno scienziato quando facciamo le migliori scarpe del mondo?" (cit.)
Re: Equilibrio termico di particelle a due stati
sì sì dovrebbe essere la "degenerazione" di uno stato, cioè la sua molteplicità quantistica (quante particelle possono coesistere simultaneamente nello stato - almeno finché consideriamo stati discreti, poi non lo so, si generalizzerà come una funzione di E in qualche modo). Tutto questo non c'entra niente col problema ovviamente.Pigkappa ha scritto:L'ho chiesto perchè ho già trovato quelleda qualche parte ma non ho mai scoperto cosa fossero. A quanto pare leggendo in quelle dispense si tratta di un coefficiente numerico che si spiega con la fisica quantistica (ergo è lecito che io non lo sappia ancora) e che non è certamente nel programma olimpico (nè ci va vicino).
